文摘
在美国,有280万急诊创伤性脑损伤(TBI)每年大约有120万人生活在大脑功能由于创伤性脑损伤的问题。虽然很多信息已经获得的实验和临床研究表明如何伤害发生,目前没有有效的治疗方法用于创伤性脑损伤。理解在大脑和脊髓创伤性脑损伤的影响,科学家们用动物模型作为一种有效的研究方法。大动物模型,如猪或羊,更接近人类身体机能。然而,使用啮齿动物模型是首选的,因为他们很容易在实验室一起工作。重要的是,这也符合国家推荐使用最低的哺乳动物的物种,可以提供科学的问题的答案。使用啮齿动物,科学家可以控制具体细节,如类型的脑损伤和损伤的严重程度。有伦理担忧受伤在科学实验的动物,但是科学家作出实质性的努力,以确保最人道的对待这些动物。最近,动物模型已经被用来发现特定的蛋白质,称为生物标记出现在创伤性脑损伤患者的大脑并可能导致新疗法的发展,以防止或减少残疾所造成创伤性脑损伤。
为什么我们需要了解创伤性脑损伤?
创伤性脑损伤(脑外伤)受伤和死亡的主要原因之一,在世界各地的各个年龄段的人。死于创伤性脑损伤的数量成千上万和伤害的数百万美元。脑外伤发生在儿童和成人通过汽车事故,瀑布,car-vs。行人受伤,爆炸伤害在军队和运动损伤。脑外伤可能一辈子都会有对一个人的生活质量的影响。接触体育喜欢足球、足球、拳击、曲棍球会导致脑外伤。重复的头部创伤可以导致的发展慢性创伤性脑病(CTE),这是大脑退化造成的重复头部受伤,导致记忆丧失和其他大脑技能。CTE与物质的积累τ蛋白在大脑中。CTE始于情绪和冲动控制问题,并逐渐发展成一场毁灭性的大脑功能丧失,类似于观察疾病如阿尔茨海默氏症和额颞痴呆。考虑到数以百万计的人,包括儿童,从事接触体育,了解创伤性脑损伤和CTE国家健康问题是一个关键。
了解创伤性脑损伤,科学家们理想的想研究创伤性脑损伤患者脑组织。然而,大脑组织样本很少患者可用的形式。大脑样本死后(死后)致命的创伤性脑损伤的病例可以被科学家研究,但是这并不足以了解疾病过程。动物模型提供一个关键方法研究创伤性脑损伤。动物模型帮助科学家研究发现治疗疾病和障碍是困难的道德研究在人类3,4]。
动物模型是什么?
动物模型是人类物种研究和比较了解常见的生物过程。动物模型中扮演重要的角色在人类创伤性脑损伤的研究。有许多种类的动物用于测试。虽然大动物对人类身体的过程更相似,啮齿动物是最常用的动物模型由于其体积小,成本低,这一事实很容易研究多个小动物在相同的实验。创伤性脑损伤的研究中使用的动物包括老鼠,棕色的老鼠,雪貂,国内猪。有些动物的大脑,可以使用类似于人类和调查机制和潜在治疗人类创伤性脑损伤(图1)[4]。
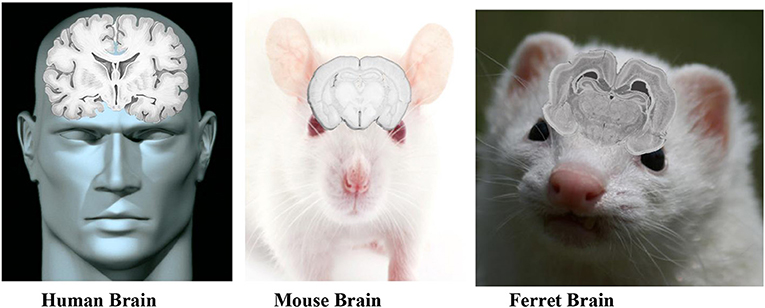
为了使创伤性脑损伤动物模型更像人类,科学家首次注入人类τ基因的动物。请注意,所有的创伤性脑损伤的研究是进行麻醉动物,所以他们不受任何痛苦之后,科学家们用不同的机制导致创伤性脑损伤的动物。不像在创伤性脑损伤的严重程度是不受控制的人类,当使用动物模型,科学家们完全控制伤害他们管理的类型,他们可以仔细测量动物的特定的生理和行为反应的创伤性脑损伤。科学家们用几种方法来产生损伤大脑,模仿那些发生给人类。不同的创伤性脑损伤模型包括产生一个局部损伤大脑,一个更广泛的损伤可能发生脑震荡的方法诱导爆炸受伤是经常出现在士兵。如上所述,动物们不觉得痛,因为他们正在麻醉和科学家是远离任何可能的伤害时执行实验。进行这些伤害动物后,科学家们收集动物的反应的数据在一个特定的时间跨度和比较他们与人类患者数据1,4,5]。
我们看看在动物模型的大脑吗?
大脑研究创伤性脑损伤,科学家常常看特定的蛋白质生物标记物。生物标志物是一种疾病过程的测量,通常测量后焦受伤吗?典型的生物标志物将血糖水平来监测糖尿病。创伤性脑损伤的生物标志物我们感兴趣包括τ蛋白、胶质原纤维酸性蛋白泛素carboxy-terminal水解酶L1,特异性神经元烯醇酶。所有这些蛋白质分子结构的一部分构成脑细胞在人类和动物模型中,像木头,拥有一所房子的框架。当有人经过外伤或受伤,这些大脑蛋白质分解,导致大脑细胞恶化,打破大脑的框架。让我们关注tau蛋白的例子。在大脑细胞叫做神经元,τ蛋白帮助构成的结构长,瘦手臂的细胞,称为轴突,沟通与其他神经元。τ扰乱脑细胞之间的通信的沉积,从而导致无序的思想和行为。τ的累积导致记忆丧失,缓慢运动,智慧,和其他破坏性的行为变化。类似于τ,列出的所有其他蛋白质也建立在大脑中以类似的方式和devasting相似效果。 Scientists have been trying to determine what leads to increases in the formation of these protein deposits and how to limit them (图2)[3,4]。
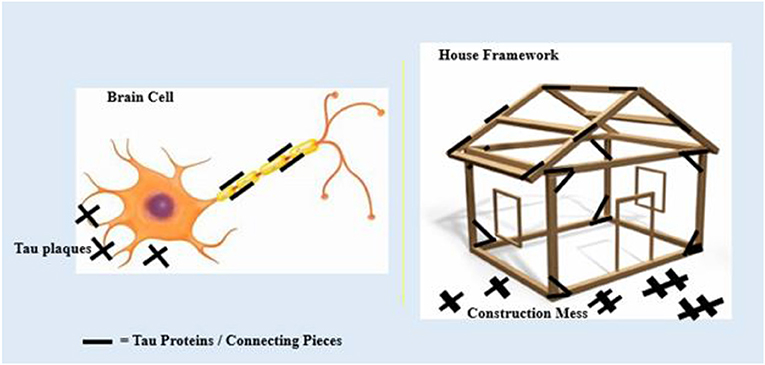
- 图2 -τ蛋白像钉子连接的框架一个木制的房子。
- τ蛋白连接的微观部分脑细胞共同创建它们的结构。在创伤性脑损伤,冲击的影响会导致τ蛋白与其他物质发生化学反应和结构。这些τ碎片收集,并形成代谢产物称为τ斑块。这些斑块导致框架周围的混乱,就像一个建筑混乱。斑块可以引起大脑的故障和导致记忆丧失、运动问题,和其他行为变化(4]。
使用动物模型的好处是什么?
使用动物模型允许研究人员调查的方式是不可能的在人类疾病的患者,因为伦理问题。人类和动物有相似的基本细胞过程,所以从动物收集到的数据可以可靠地预测人类相似的结果。动物研究还允许科学家收集数据从许多不同的动物,从而增加研究结果的可靠性。一些实验动物,如老鼠,在大量繁殖,所以有很多老鼠用于研究。
有很多讨论是否正确或错误使用动物进行研究。有些人认为没有足够的确凿的证据比较动物模型与人类的模型。但是其他的人认为在研究中使用动物是唯一的方法来了解一些人类疾病和找到解决这些疾病。创伤性脑损伤的研究中,这项新研究等τ生物标记,帮助我们检测潜在的更好的诊断为脑震荡,不会在理解创伤性脑损伤提供了一个突破不使用动物模型。人类只使用事后样品没有提供足够的数据来测试科学理论对创伤性脑损伤的生物标志物扮演的角色。动物模型帮助我们研究人类系统更快更有效的方法。
很多人争取动物的道德权利,认为动物应该没有被实验对象时的痛苦。保持道德实践,科学家建立了监管董事会有关动物研究执行一组严格的规则。有科学家可以和不能做的事情,什么类型的研究动物模型可以和不能使用的。这些规则支持三个R:替换,减少和改进。科学家必须组织他们的实验,这样他们取代动物与其他无动物选择尽可能经常。此外,科学家必须计划他们的实验,这样他们使用的动物数量减少到最小的可能的数字,会给他们足够的证据的研究问题。最后,科学家必须细化程序完成对动物减少过度伤害或l遇险的动物。这些规章制度允许科学家取得好结果影响最少的动物。有重大突破在理解人类疾病使用动物模型,但希望,随着技术的进步,科学家将逐渐可以用越来越少的动物的研究(1,5]。
结论
动物模型是为许多类型的科学家研究必不可少的工具。科学家研究大脑的像我们这样,动物帮助我们调查最为复杂的器官之一。动物模型帮助我们研究疾病的关键特性,使用人体难以调查。这些模型可以帮助我们理解某些蛋白质的积累的过程,像τ,大脑的损害大脑的结构和功能。根据这些信息,科学家们正在努力发现方法来限制τ累积,进而减少CTE等严重疾病的影响,阿尔茨海默氏症,帕金森氏症和其他禁用大脑的疾病。
术语表
创伤性脑损伤(TBI):↑脑损伤引起的强烈的伤害直接针对头部,造成的事故,体育,和其他创伤。
慢性创伤性脑病(CTE):↑大脑退化造成的重复的头部受伤,导致进步的损失在大脑记忆和其他技能。
τ蛋白:↑蛋白质存在于大脑里的神经元,帮助神经元保持适当的结构。
死后:↑死后病人或主题。
动物模型:↑动物用于研究疾病的发展和进展和测试新的治疗方法之前给人类。
道德:↑有关对与错的问题。
生物标志物:↑一个分子显示是否有疾病或其他问题。
焦受伤:↑局部组织损伤引起的直接的力量。
的利益冲突
作者声明,这项研究是在没有进行任何商业或财务关系可能被视为一个潜在的利益冲突。
引用
[1]↑戴,j . X。,Ma, Y. B., Le, N. Y., Cao, J., and Wang, Y. 2018. Large animal models of traumatic brain injury.Int。j . >。128:243-54。doi: 10.1080 / 00207454.2017.1380008
[2]↑罗杰斯,s . 2019。大思想家。Simonrogersdotnet.files.wordpress.com。网上:https://simonrogersdotnet.files.wordpress.com/2014/03/brain-size.png(2019年11月4日通过)。
[3]↑王,J。苏E。,Wang, H., Guo, C., Lawrence, D. A., and Eitzman, D. T. 2018. Traumatic brain injury leads to accelerated atherosclerosis in apolipoprotein E deficient mice.科学。代表。8:5639。doi: 10.1038 / s41598 - 018 - 23959 - 2
[4]↑Whitwell, j·L。,and Josephs, K. A. 2013. “Tauopathies,” in Magnetic Resonance Imaging in Movement Disorders: A Guide for Clinicians and Scientists, ed P. Tuite (Cambridge University Press). p. 147–66. doi: 10.1017/CBO9781139207294.014
[5]↑熊,Y。,Mahmood, A., and Chopp, M. 2013. Animal models of traumatic brain injury.Nat。启>。14:128-42。doi: 10.1038 / nrn3407

